尚维高科自主研发的产品于近期再次获CE欧盟市场、美国FDA准入资格。
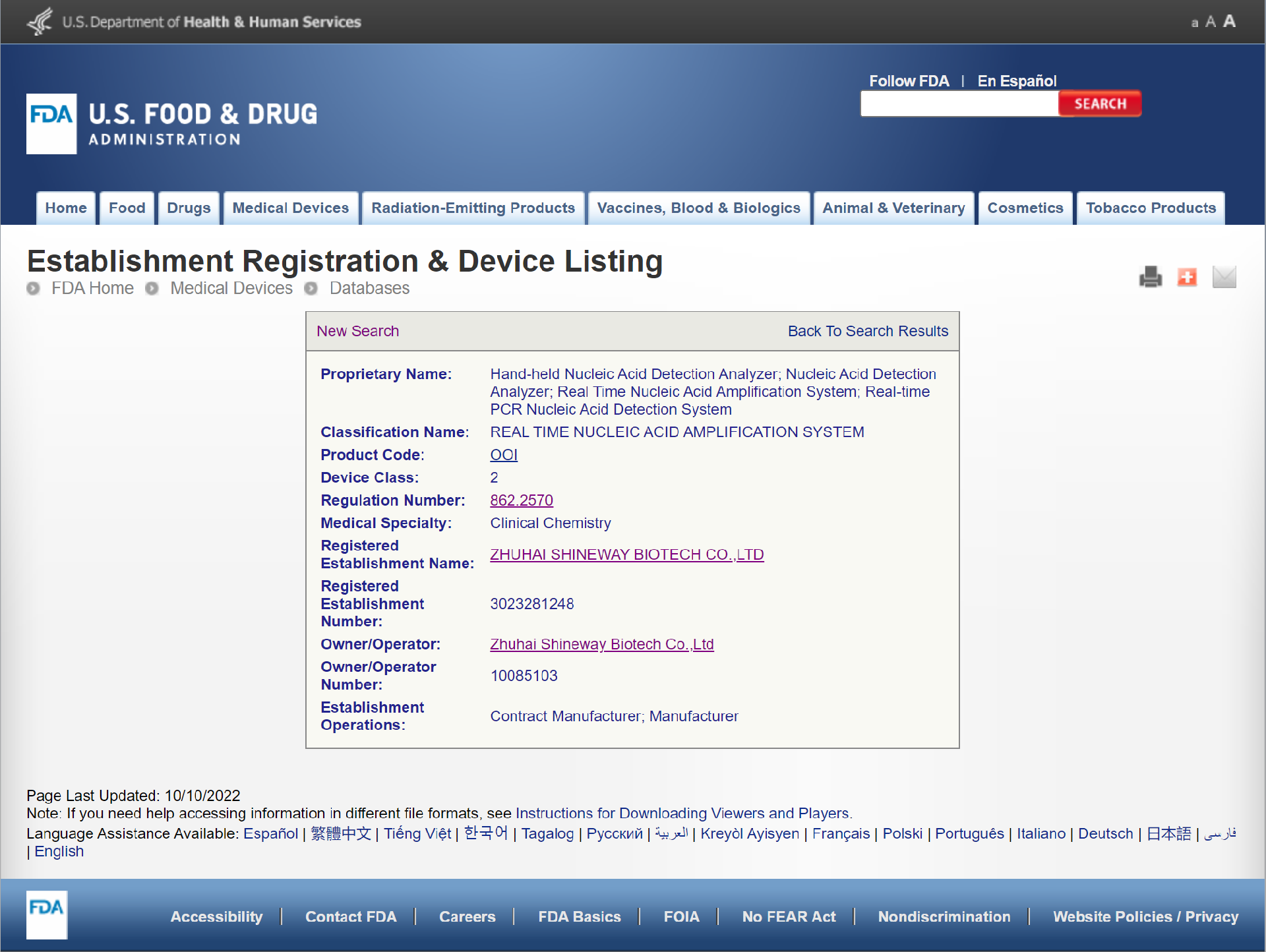
▲美国FDA认证
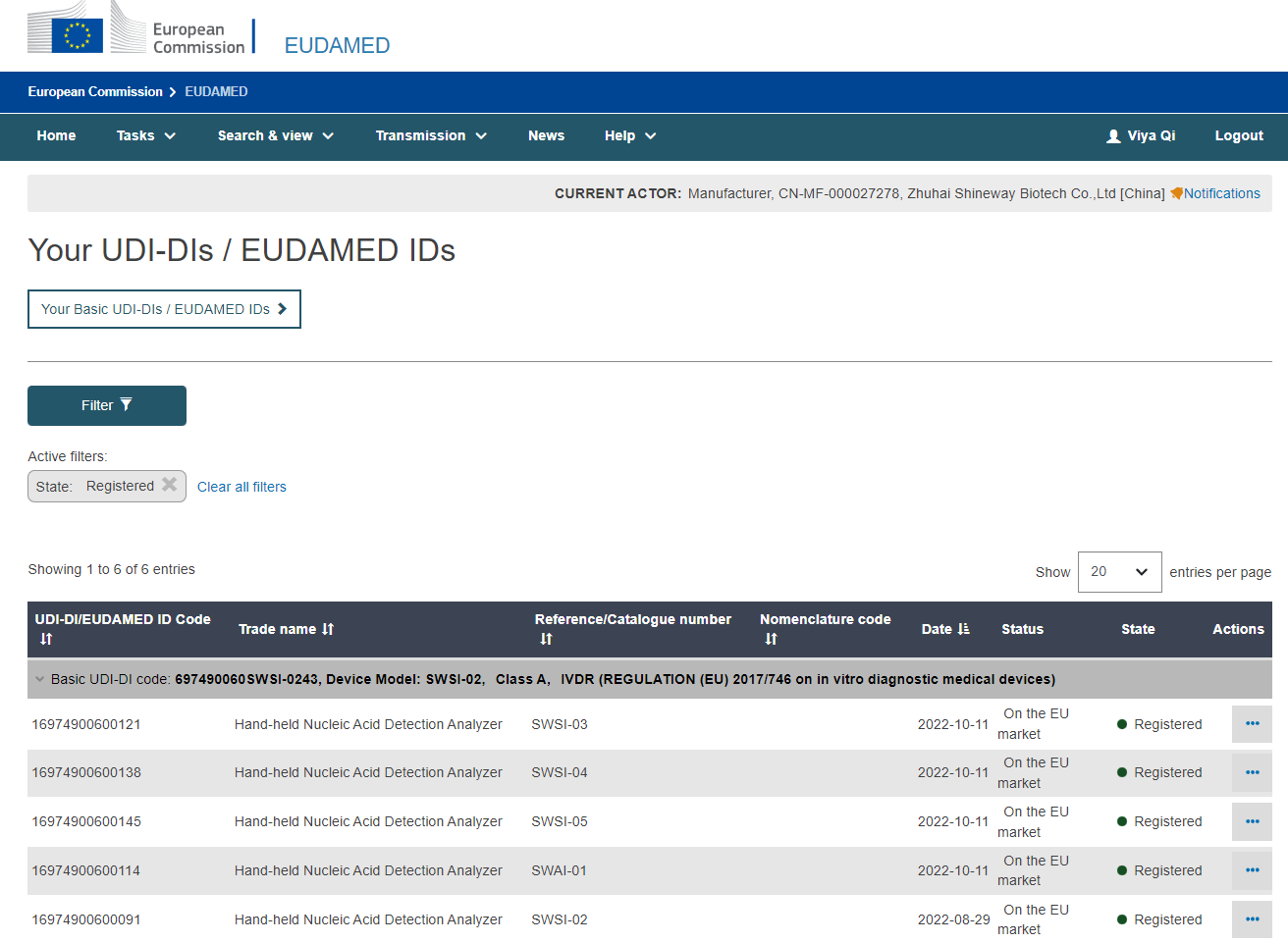
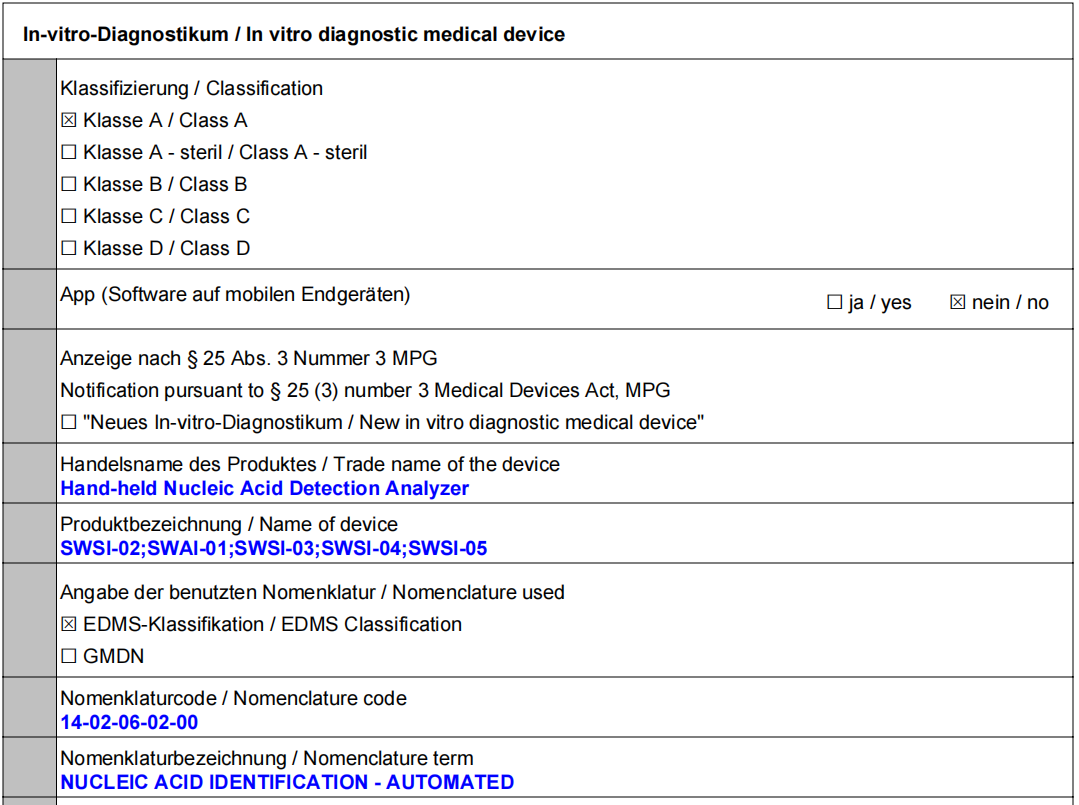
▲欧盟IVDR认证
本次获得认证的产品是手持式核酸检测仪(Hand-held Nucleic Acid Detection Analyzer),包含多个不同用途的型号款式,该产品基于等温核酸扩增技术,与指定的IVD试剂共同使用,实现即采即测,无需样本转运,可连接手机30分钟后一键查看结果,居家亦能使用,操作便捷,应用场景随意切换。

▲手持式产品,小巧灵活
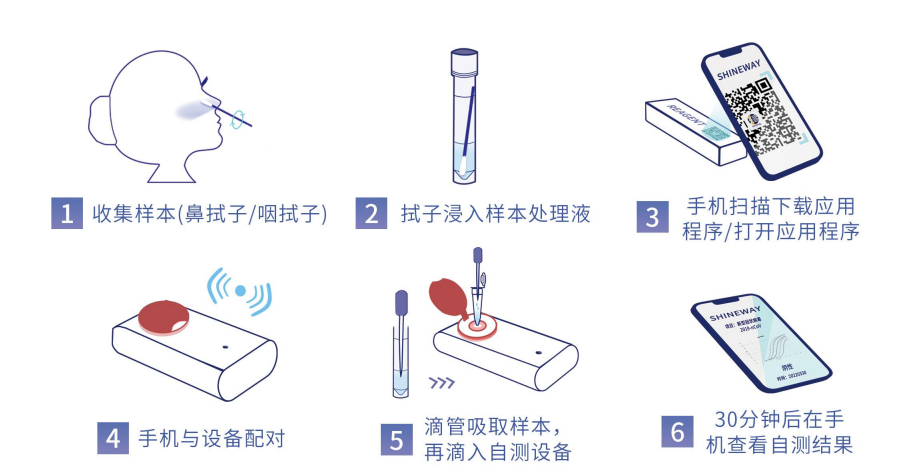
▲便捷的操作流程

▲图为产品概览
产品多次获得国际认证,不仅验证了尚维高科对高标准的遵守,还突破了产品工艺技术的挑战。我们专注于体外诊断领域的研发与技术积累,持续重视研发投入,已积累沉淀扎实的研发实力和创新能力,未来也将加快推进成果转化,为国内及世界体外诊断发展作出更大贡献。
*关于FDA
FDA是美国食品药物管理局(U.S.Food and Drug Administration)的英文缩写,它是国际医疗审核权威机构,由美国国会即联邦政府授权,通过FDA认证的医疗器械对人体是确保安全而有效的。
*关于IVDR
对于A类产品来说,通过IVDR注册是进入欧盟市场的必要条件。2017年4月5日欧盟正式签发的新版体外诊断医疗器械法规IVDR(EU 2017/746),相对于旧指令,新法规无论从上市前申请或上市后监督都进行了大规模的修订,内容更全面系统。随着 UDI 的实施和 EUDAMED 数据库的建立,新 IVDR 法规下上市的产品将实现全球多方全生命周期的监管,实现产品动态实时追踪的可能。这也标志着欧盟当局对医疗设备领域监管的进一步重视,同时也预示着在欧盟各成员国内医疗器械监管的尺度将得到进一步的统一。